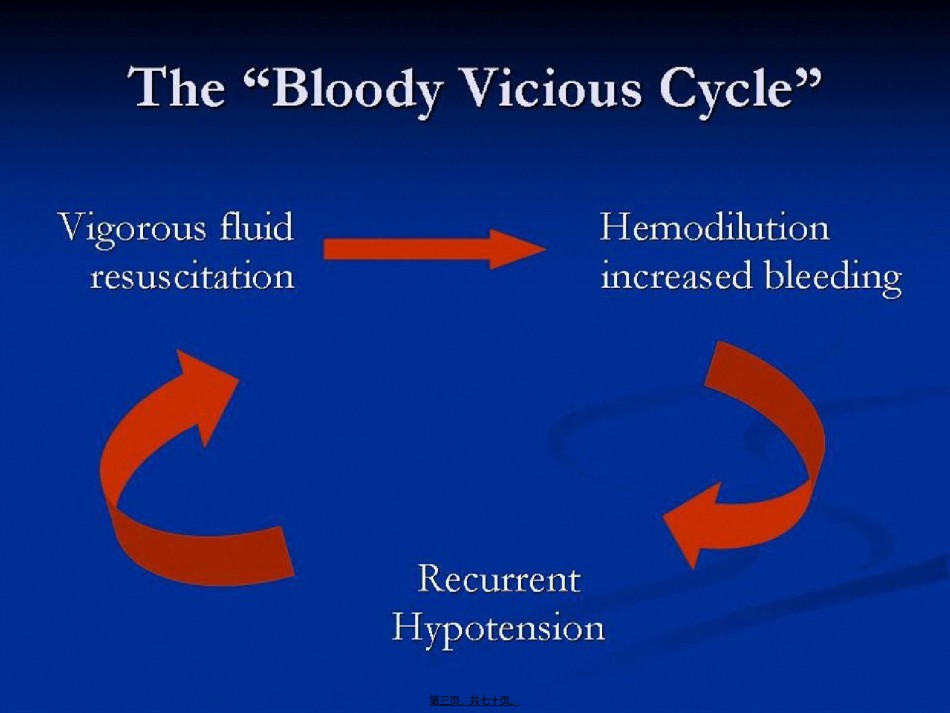
创伤性出血(chūxiě)控制第一页,共七十页。第二页,共七十页。第三页,共七十页。•大出血是院前创伤患者仅次于中枢神经系统损伤的死亡因素(yīnsù)。•手术及创伤:占“DIC”的5%-10%。•院内创伤患者约40%由于不能控制的出血在最初48小时内死亡。凝血障碍、低温和代谢性酸中毒(thelethaltriad)低灌注、血流动力学不稳定、呼吸困难和感染第四页,共七十页。创伤性出血(chūxiě)创伤性凝血病(Thecoagulopathyoftrauma)指严重创伤后发生于粘膜损伤处、浆膜面、手术创面及导管置入部位等非外科性出血,常伴有低温、酸中毒、血液稀释,偶尔与典型的DIC一同出现,同低温对血小板的影响、PH值对凝血因子活力的影响及常规液体复苏(fùsū)后的血液稀释有关。创伤性DIC急性DIC常指脑、脂肪组织、羊水或其它强促凝物质在创伤过程中入血所诱发的DIC。亚急性DIC多发生于血管内皮细胞炎症反应或机体不能及时清除促凝因子而大量形成微小血栓所导致的DIC。Hess,Thecoagulopathyoftraumaversusdisseminatedintravascularcoagulation.J-Trauma.2006Jun;60(6Suppl):S12-9第五页,共七十页。血管收缩第六页,共七十页。大量组织破坏,组织因子进入血液血管内皮下成分暴露伴发休克、感染,可激活外源、内源凝血系统(xìtǒng)红细胞破坏、血小板破坏输入大量库血接触富含促凝血酶原激酶(thromboplastin)的脑组织、肺组织启动炎症反应瀑布启动免疫反应瀑布(chuāngshāng)第七页,共七十页。第八页,共七十页。•TNF和IL-1通过抑制血栓调节蛋白(TM)的表达以及(yǐjí)活化蛋白C(APC)的生成,解除对凝血反应的抑制。•TNF和IL-1使内皮细胞组织型纤溶酶原激活物(tPA)的合成减少,却增加组织型纤溶酶原激活物抑制剂(tPAI)的合成。蛋白C(PC)能抑制tPA的活性。•IL-10能下调LPS诱导的单核细胞组织因子(MTF)mRNA的转录、蛋白质的表达及促凝活性,以限制最初过度的炎症反应中DIC的发展。第九页,共七十页。临床(línchuánɡ)发现Gando发现进展为DIC的创伤患者其ISS评分明显高于非DIC患者,最初12小时(xiǎoshí)血中TNF-a和IL-1水平均高。创伤后DIC患者TF及PAI-1水平在5天内都升高,凝血与纤溶均亢进。这些患者TM水平升高,而APC水平下降。GandoS.Systemicactivationoftissue-factordependentcoagulationpathwayinevolvingrespiratorydistresssyndromeinpatientswithtraumaandsepsis.JTrauma1999;47:719-23.第十页,共七十页。AT-Ⅲ:主要抑制凝血酶及因子Ⅶa、Xa、IXa、XIa和XⅡa活性,肝素协同其作用。肝素辅因子-Ⅱ:作用类似AT-Ⅲ,但只抑制凝血酶,其协同物不仅有肝素,还有硫酸(liúsuān)皮肤素。凝血酶调节蛋白(TM):它与凝血酶分子表面的阴离子结合,改变了凝血酶分子的构象,即由促凝物变为抗凝物。蛋白C(PC)和蛋白S(PS):PC是一种相当重要的天然抗凝物,它经TM/凝血酶复合物活化后形成活化的PC(APC),可灭活(降解)FⅧa和FVa,从而起到抗凝作用。PS可加强和促进PC的作用。组织因子通路抑制剂是另一种调节蛋白,它与因子Ⅹa结合能灭活组织因子-Ⅶ复合物。第十一页,共七十页。•持续的出血和无选择的纤维蛋白凝结是凝血问题的两个极端,创伤对两者都是高危因素,在决定体内凝血进程时,纤溶的作用强于凝血,创伤尤其如此,受伤部位是否能形成血栓,要视血栓抑制剂而定,多发(duōfā)伤导致广泛的凝血因子激活,结果出现不受控制的纤溶。第十二页,共七十页。代凝低血谢血温液性因稀酸子释中消毒耗(xīshì)(代谢障碍)第十三页,共七十页。输入(shūrù)超过1.5倍自身危险值血容量Fibrinogen:1.0g/L—替换(tìhuàn)142%当给予10-12个单位血液纤维蛋白原小于80时血小板明显下降,血液mg/dL会引起PT-INR稀释可能是个原因和APTT延升,而小于50mg/dL则会出抗凝血酶Ⅲ,蛋白C、蛋白血不止S下降(xuèyè)FactorⅤ、Ⅶ---替换201-236%第十四页,共七十页。低温Helm监测了一个创伤中心中94例插管患者的体温,发现其中2/3的病人中心温度(wēndù)小于36℃。℃以中心体温低于34℃生存率将明显下降。低温:体温低于35℃。创伤低温34-36℃---轻度...